Биологически активные добавки к пище (БАД) – неотъемлемый элемент здорового питания современного человека.
Безопасность БАДов для организма строго контролируется на государственном уровне. Ещё до предложения потребителю такой товар проходит обязательные лабораторные исследования, результаты которых оформляются в виде Протоколов испытаний.
Протоколы испытаний необходимы для государственной регистрации БАДов и разрешения их выпуска на рынок России и других стран ЕАЭС.
Оформляем легитимные Протоколы испытаний БАД для получения Свидетельства о государственной регистрации (СГР) и занесения товара в Единый реестр специализированной пищевой продукции.
Под требования каких технических регламентов попадают БАДы?

Пищевые биодобавки не относят к лекарственными средствами.
Являясь специализированными продуктами питания, они попадают под действие технического регламента таможенного союза «О безопасности пищевой продукции» (ТР ТС 021/2011).
Полный перечень всех 46-ти ТР ТС
Маркировка упаковки и объём обязательной информации, размещённой на этикетке и листке-вкладыше БАД, контролируется техническим регламентом таможенного союза «Пищевая продукция в части её маркировки» (ТР ТС 022/2011)
ТР ТС 021/2011 - какие требования предъявляются к БАДам?
Подтверждение соответствия безопасности БАДов требованиям ТР ТС 021/2011 проводится в форме государственной регистрации с выдачей СГР
Общие требования к безопасности БАД, установленные настоящим техрегламентом:
- БАДы, распространяемые на территории РФ/ЕАЭС и применяемые по назначению, должны быть безопасны для потребителя на протяжении всего установленного срока годности
- Производство, хранение и распространение БАДов на территории РФ/ЕАЭС разрешено только после их государственной регистрации в порядке, установленном ТР ТС 021/2011
- В БАДах не должно обнаруживаться токсичных, болезнетворных и других опасных компонентов, способных нанести вред человеку и окружающей среде
- Показатели безопасности, определяемые в ходе лабораторных испытаний, должны соответствовать гигиеническим требованиям, установленным в Приложениях 1, 2, 3 к ТР ТС 021/2011
- Для производства БАДов недопустимо использовать растения, объекты животного или другого происхождения, а также продукты их переработки, опасные для жизни и здоровья человека, перечисленные в Приложении 7 к настоящему техрегламенту
- Содержание активных биологических веществ в суточной норме БАДов должно быть меньше 50% от установленной величины их разовой лечебной дозы
- Исследование образцов БАД на соответствие нормативным документам могут осуществлять только аккредитованные в профильной области испытательные лаборатории (Центры)
Контролируемые микробиологические показатели безопасности БАД:
- Мезофильные аэробные и факультативно-анаэробные микроорганизмы
- Колиформы (бактерии группы кишечных палочек)
- Эшерихии коли (E. coli)
- Золотистый стафилококк
- Плесени
- Дрожжи
- Живые клетки продуцента биологически активных компонентов
- Бациллы токсикоинфекций человека
- Мезофильные аэробные и факультативно-анаэробные микроорганизмы
- Колиформы (бактерии группы кишечных палочек)
- Эшерихии коли (E. coli)
- Золотистый стафилококк
- Плесени
- Дрожжи
- Живые клетки продуцента биологически активных компонентов
- Бациллы токсикоинфекций человека
ТР ТС 022/2011 - какие требования предъявляются к БАДам?
1. Упаковка и/или этикетка на упаковке биоактивной добавки в обязательном порядке должна нести исключительно правдивые сведения следующего содержания:
- наименование БАД
- сведения о назначении
- состав
- количество (мл, граммов, штук)
- дата производства
- срок годности
- условия хранения
- рекомендации по применению
- показатели пищевой ценности в процентном отношении к величинам, отражающим среднесуточную потребность взрослого человека в белках, жирах, углеводах, энергии, витаминах, минеральных и других веществах в соответствии с Приложением 2 ТР ТС 022/2011
- сведения о наличии/отсутствии в продукте ГМО
- сведения об изготовителе продукции в объёме, установленном настоящим техрегламентом
- регистрационный номер и дата выдачи СГР
- единый знак обращения на рынке «ЕЭС»
2. Состав и качественные характеристики БАД, указанные на упаковке, этикетке, листке-вкладыше должны соответствовать фактическому составу и качественным характеристикам продукта, размещённого в потребительской упаковке
Классификация БАДов

Биоактивные пищевые добавки подразделяют на:
- Витамины
- Минералы
- Аминокислоты
- Комплексные (витаминно-минеральные и т.п.)
- Незаменимые жирные кислоты
- Спортивные БАД (добавки для спортивного питания)
- Пробиотики
- Пребиотики
- Добавки из натурального растительного сырья
- Добавки из натурального сырья животного происхождения
- Продукты пчеловодства
- Пищевые волокна
- Суперфуды (суперпища)
- Адаптогены
- Иммуномодуляторы
- и мн.др.
Процедура лабораторных испытаний БАДов

Этапы проведения испытаний БАД в наших аккредитованных лабораториях:
- Подача Заказчиком Заявки на испытания конкретного объекта
- Предоставление Заказчиком необходимой документации на продукцию
- Составление Договора на услуги лаборатории
- Отбор образцов продукции для испытаний
- Идентификация объекта испытаний
- Проведение лабораторных исследований в объёме, предусмотренном техрегламентом, достаточном для оценки безопасности БАД в рамках дальнейшей государственной регистрации
- Оформление результатов выполненных работ в виде Протоколов испытаний
- Регистрация Протоколов в Реестре лаборатории-исполнителя
- Бесплатная доставка готовых документов Заказчику
Когда необходимости в проведении лабораторных испытаний нет?
Обязательные лабораторные испытания БАД являются этапом процедуры подтверждения соответствия продукции требованиям технических регламентов таможенного союза в форме государственной регистрации.
Срок действия СГР, выданного на конкретный вид биодобавки, не ограничен.
Поэтому БАДы:
- успешно прошедшие государственную регистрацию,
- занесённые в Единый реестр специализированной пищевой продукции,
- выпускаемые баз каких-либо изменений в рамках действующего законодательства,
повторным лабораторным испытаниям не подлежат.
Какие документы необходимо предоставить Заказчику?
- Заявка на лабораторные испытания продукции
- Реквизиты Заказчика, ОГРН, ИНН
- Сведения об изготовителе БАД, включая полное наименование и адрес фактического местонахождения производства
- Техническая документация на продукцию (ТУ, др.)
- Другие документы – по требованию и согласованию с лабораторией
Какие данные заносятся в Протокол испытаний?
Обязательные сведения, которые заносятся в Протокол испытаний БАД:
- Полное наименование испытательной лаборатории, юридический и фактический, контакты, уникальный номер записи об аккредитации в Реестре аккредитованных лиц
- Отметка об утверждении документа за подписью руководителя испытательной лаборатории
- Название документа (Протокол испытаний), его уникальный номер и дата регистрации
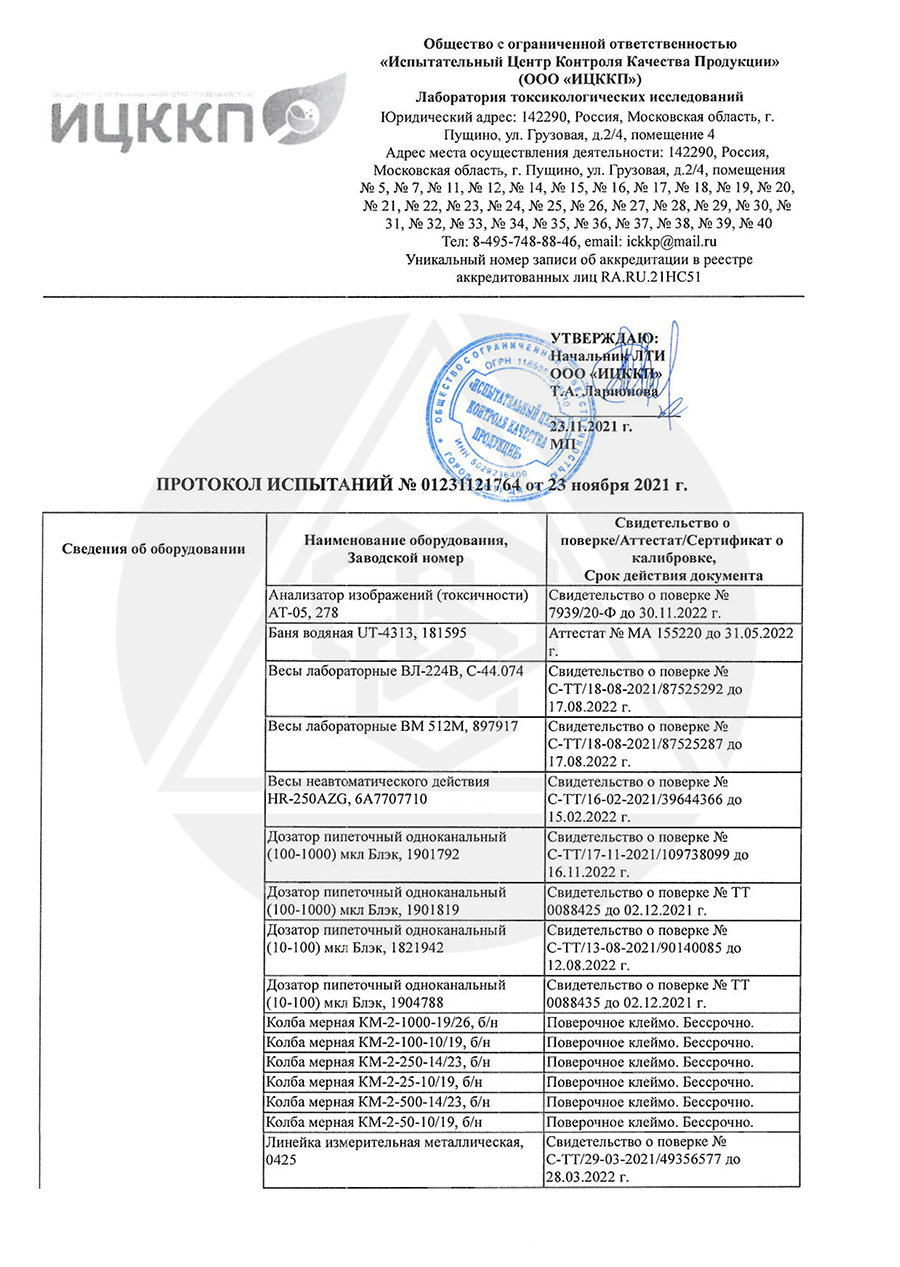
- Наименование и сведения об аттестации оборудования, использованного в ходе испытаний
- Наименование образца продукции, доставленного для испытаний
- Идентификационный код испытуемого образца
- Наименование и адрес предприятия-изготовителя
- Наименование и адрес Заявителя испытаний
- Сведения о Заявке на испытание
- Дата отбора образцов продукции
- Дата поступления отобранных образцов в лабораторию
- Дата начала и окончания проведения испытаний
- Результаты испытаний, представленные в виде таблицы:
| Определяемый показатель, единицы измерения | Норматив, утверждающий метод испытаний/измерений | Результат испытаний | Норма показателя по нормативному документу | Обозначение нормативного документа | Заключение о соответствии |
|---|---|---|---|---|---|
| *** | ГОСТ ___ | *** | *** | ТР ТС ___ | *** |
- Условные обозначения
- Примечания
- ФИО и подпись ответственного за оформление протокола
- Отметка о завершении документа (Конец протокола)
Аккредитованные испытательные лаборатории нашего многофункционального Центра ООО «ЦСД», в том числе лаборатория токсикологических исследований ООО «ИЦККП»:
- оформляем Протоколы испытаний продукции на фирменных бланках организации;
- готовые Протоколы соответствуют всем требованиями российского законодательства, ГОСТ Р 58973-2020, ГОСТ ISO/IEC 17025;
- гарантируем полную легитимность всех выданных документов;
- работаем без посредников, быстро, качественно, исключительно в правовом поле.
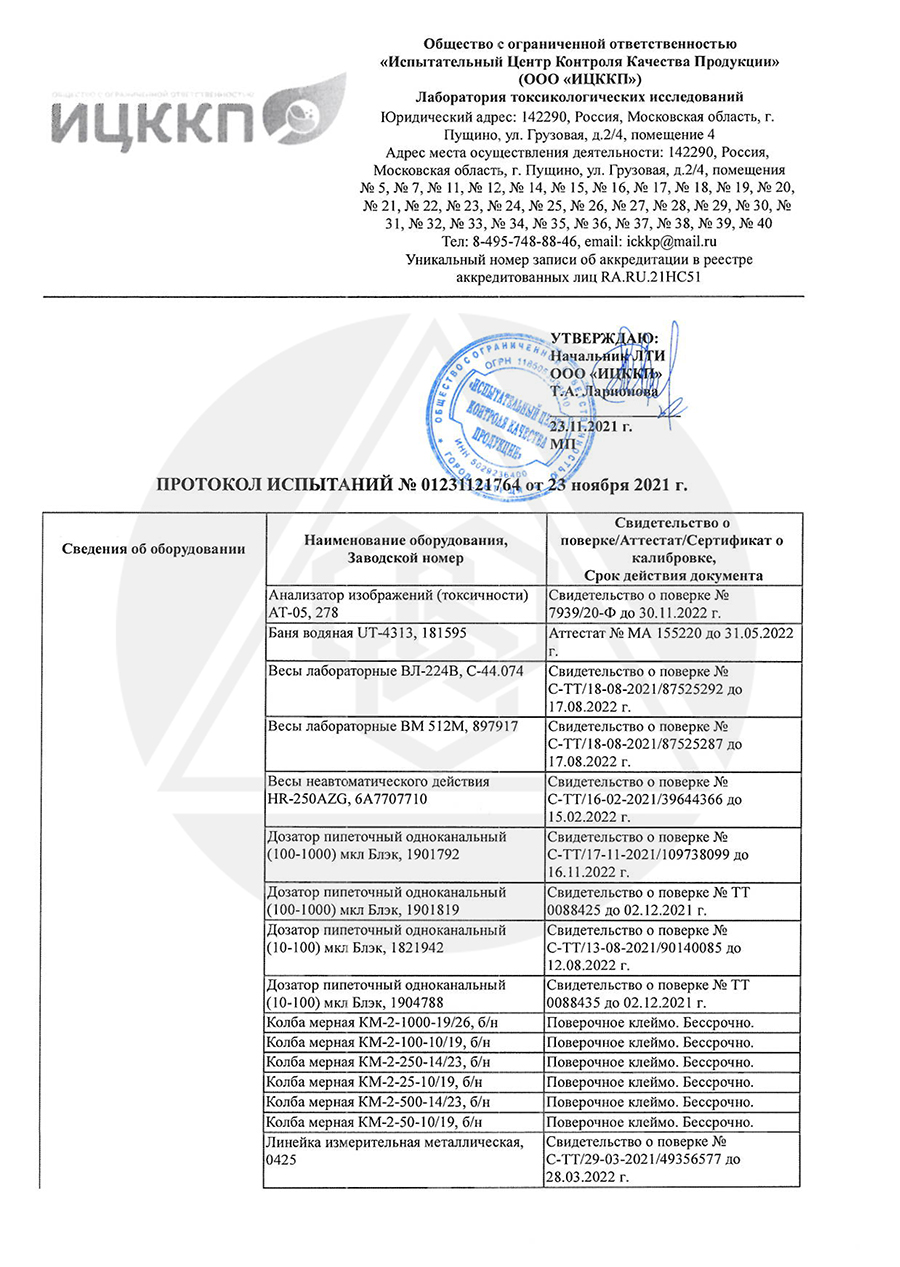
Для получения протокола испытаний требуется
Учредительные документы,
Реквизиты заявителя,
Заявление,
Техническая документация
Аттестат аккредитации RA.RU.21HP36
Аттестат аккредитации RA.RU.21HA14
Аттестат аккредитации RA.RU.21HC51